藍細菌賴氨酸巴豆酰化調控酶的鑒定與功能機制研究進展
賴氨酸巴豆酰化修飾是生物體內重要的蛋白質翻譯后修飾之一,指的是巴豆酰基團從巴豆酰輔酶A (crotonyl-CoA) 轉移到蛋白質特定的賴氨酸ε-氨基上,形成巴豆酰化的賴氨酸。這種修飾因其獨特的四碳結構和由碳-碳π鍵形成的剛性平面結構而區別于其他酰基化修飾,它能夠顯著影響蛋白質與DNA及蛋白質間的相互作用,進而在基因表達調控、代謝途徑調節等眾多生物學過程中扮演重要角色。研究表明,賴氨酸乙酰轉移酶和去乙酰化酶也參與調控巴豆酰化修飾的過程。中國科學院水生生物研究所葛峰研究員聯合趙進東院士團隊先前已報道了藍細菌中首個賴氨酸乙酰轉移酶和去乙酰化酶,這些酶通過調控底物的乙酰化狀態影響藍細菌的生長和光合作用(Plant Physiology,2020,184(2):762-776;Plant Physiology,2023,194(2):634-661)。圍繞藍細菌中是否存在特定的賴氨酸巴豆酰化調控酶這一問題,研究人員開展了深入研究。
近期,該研究團隊在藍細菌Synechococcus sp. PCC 7002中系統篩選潛在賴氨酸巴豆酰轉移酶。通過體內外實驗證實,乙酰轉移酶cGNAT2兼具巴豆酰轉移酶活性。分析表明,cGNAT2與乙酰輔酶A和巴豆酰輔酶A的結合位點存在空間差異,且其催化乙酰化和巴豆酰化反應的活性位點互不重疊,提示該酶通過差異化催化機制介導兩類修飾(圖1)。
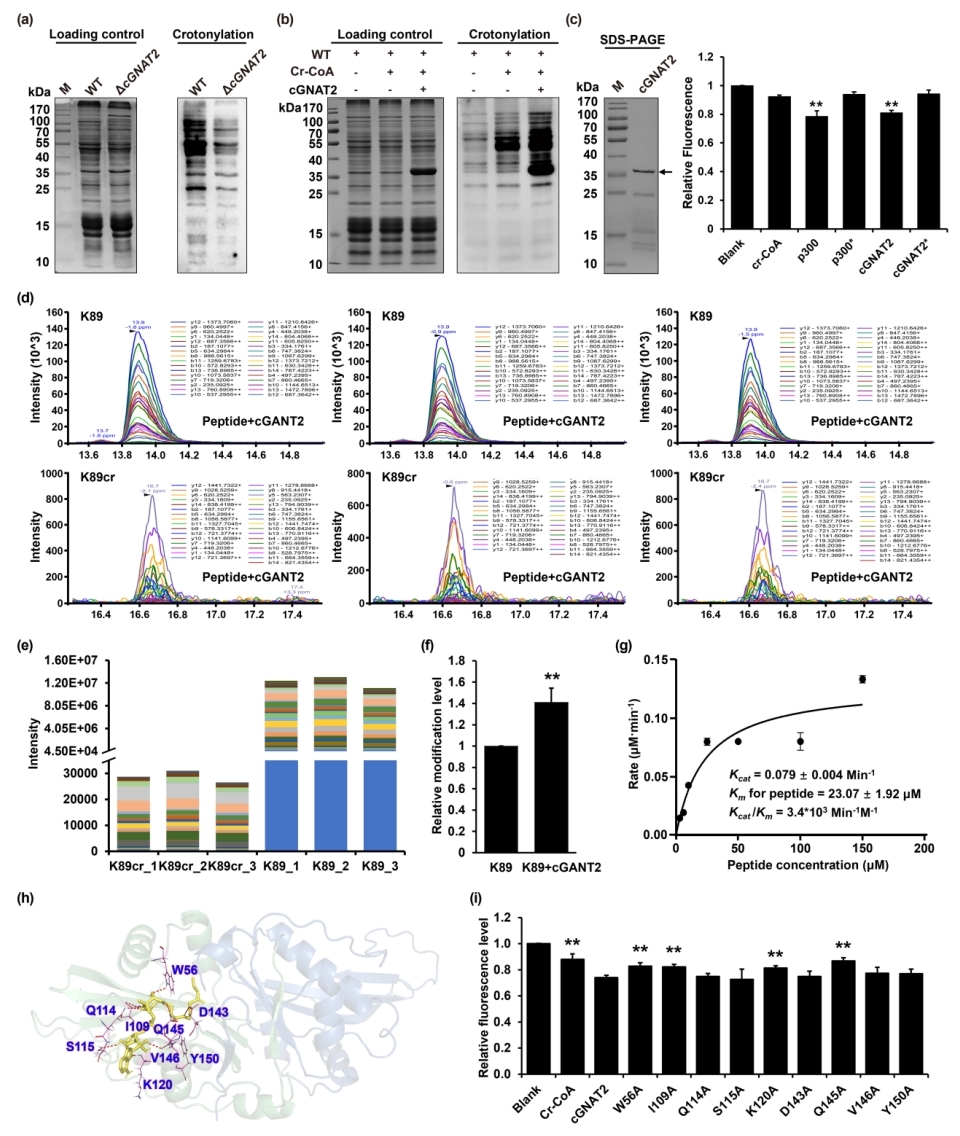
圖1. 藍細菌賴氨酸巴豆酰轉移酶cGNAT2的鑒定和結構分析
研究團隊對Synechococcus sp. PCC 7002中的去乙酰化酶也進行了系統篩選。通過體內外實驗證實,Synechococcus sp. PCC 7002中的去乙酰化酶CddA同樣具有去巴豆酰化能力,可有效去除藍細菌和大腸桿菌蛋白的巴豆酰化修飾,對CddA的催化活性位點突變分析發現,該酶的催化活性具有位點特異性(圖2)。
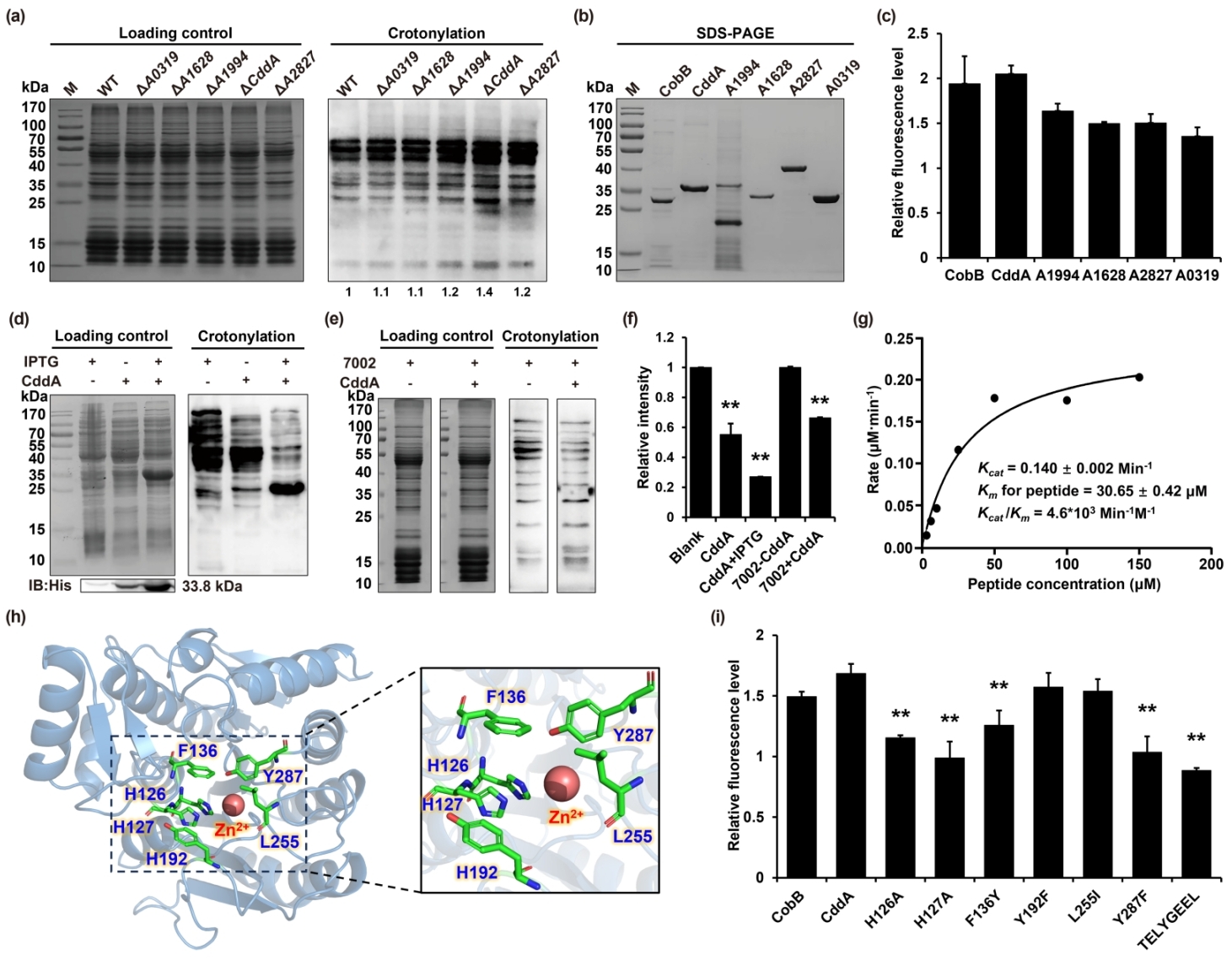
圖2. 藍細菌賴氨酸去巴豆酰化酶CddA的鑒定和結構分析
為深入理解cGNAT2和CddA的分子作用機制,研究團隊采用巴豆酰化抗體富集和非標記定量巴豆酰化組學技術,鑒定到536個cGNAT2靶標修飾蛋白和360個CddA底物蛋白。這些蛋白廣泛分布于代謝途徑和光合作用通路中,較多代謝關鍵酶受到cGNAT2和CddA的協同調控,表明cGNAT2和CddA介導的巴豆酰化修飾在光合作用和能量代謝等過程中具有重要的調控作用(圖3)。
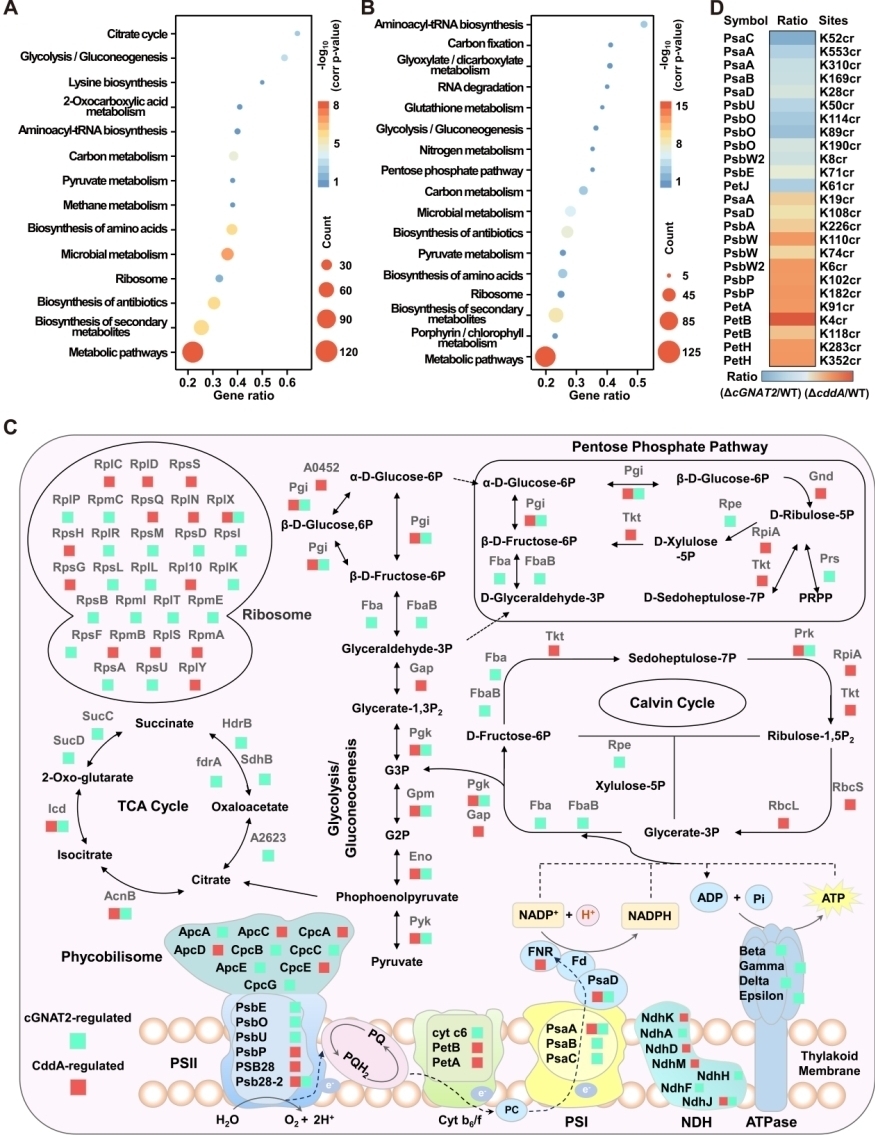
圖3. cGNAT2和CddA的內源性靶標蛋白鑒定
功能實驗表明,光系統I蛋白(PsaD)是cGNAT2和CddA的關鍵作用標靶,cGNAT2特異性催化PsaD的K28位巴豆酰化,而CddA介導K108位的去巴豆酰化。通過體外酶促反應、生物膜干涉實驗和體內的免疫共沉淀實驗,研究進一步驗證了cGNAT2和CddA能夠在體內外調控PsaD的巴豆酰化修飾狀態(圖4)。
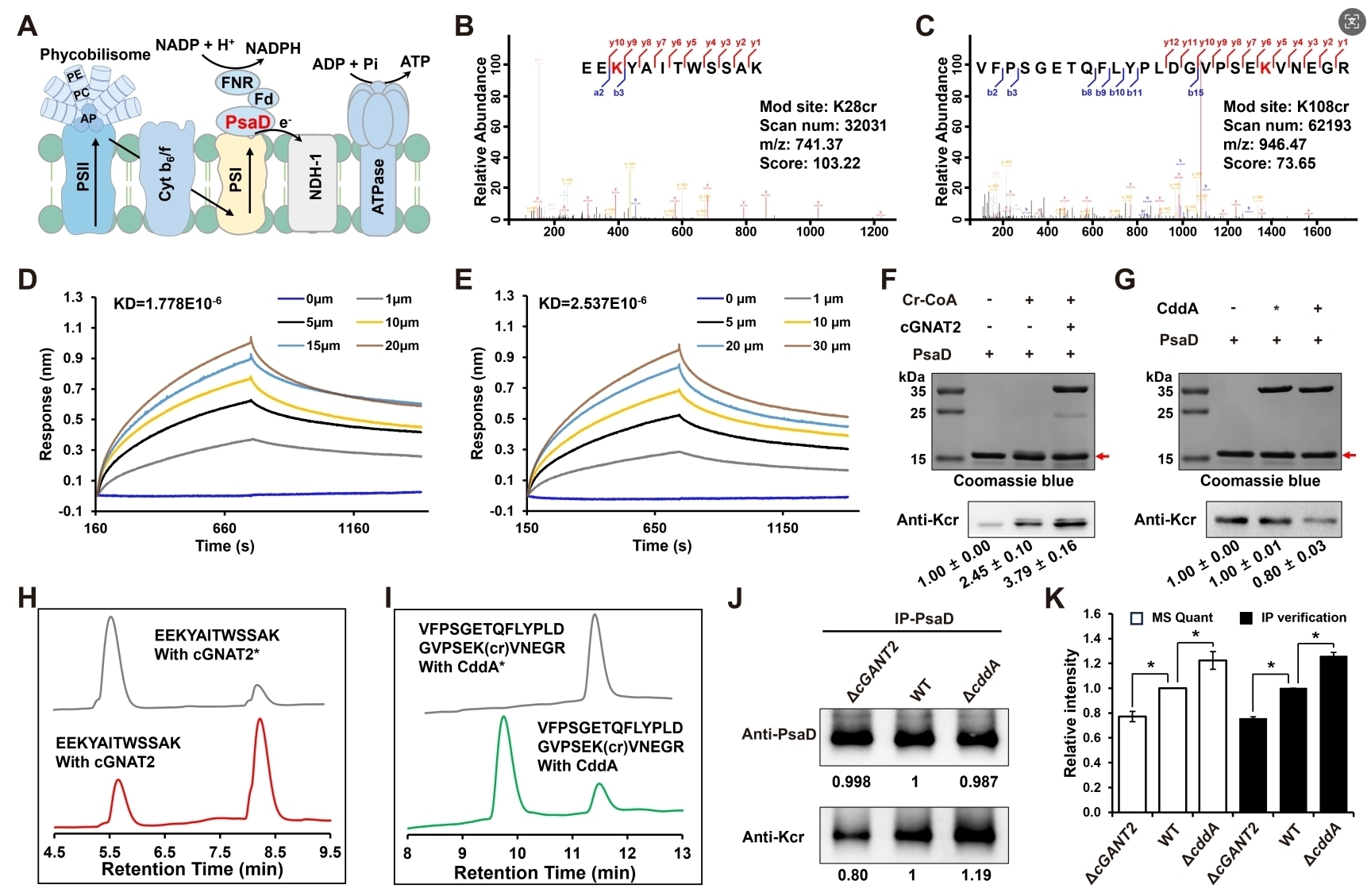
圖4. cGNAT2和CddA調控PsaD的巴豆酰化
為探索巴豆酰化對PsaD功能的調控機制,研究團隊構建了PsaD的修飾位點突變菌株。表型分析顯示,在正常光照和高光脅迫條件下,突變株的生長速率和光合作用效率受到顯著影響,表明K28和K108巴豆酰化修飾的動態平衡可能影響光系統I的穩定性,從而影響藍細菌的生長和光合作用過程。
該研究首次在藍細菌中發現賴氨酸巴豆酰轉移酶cGNAT2和去巴豆酰化酶CddA,并闡明其通過特異性調控底物蛋白的巴豆酰化修飾進而實現其功能的分子機制(圖5),為研究藍細菌以及其他光合生物的光合作用調控機制提供了新思路。
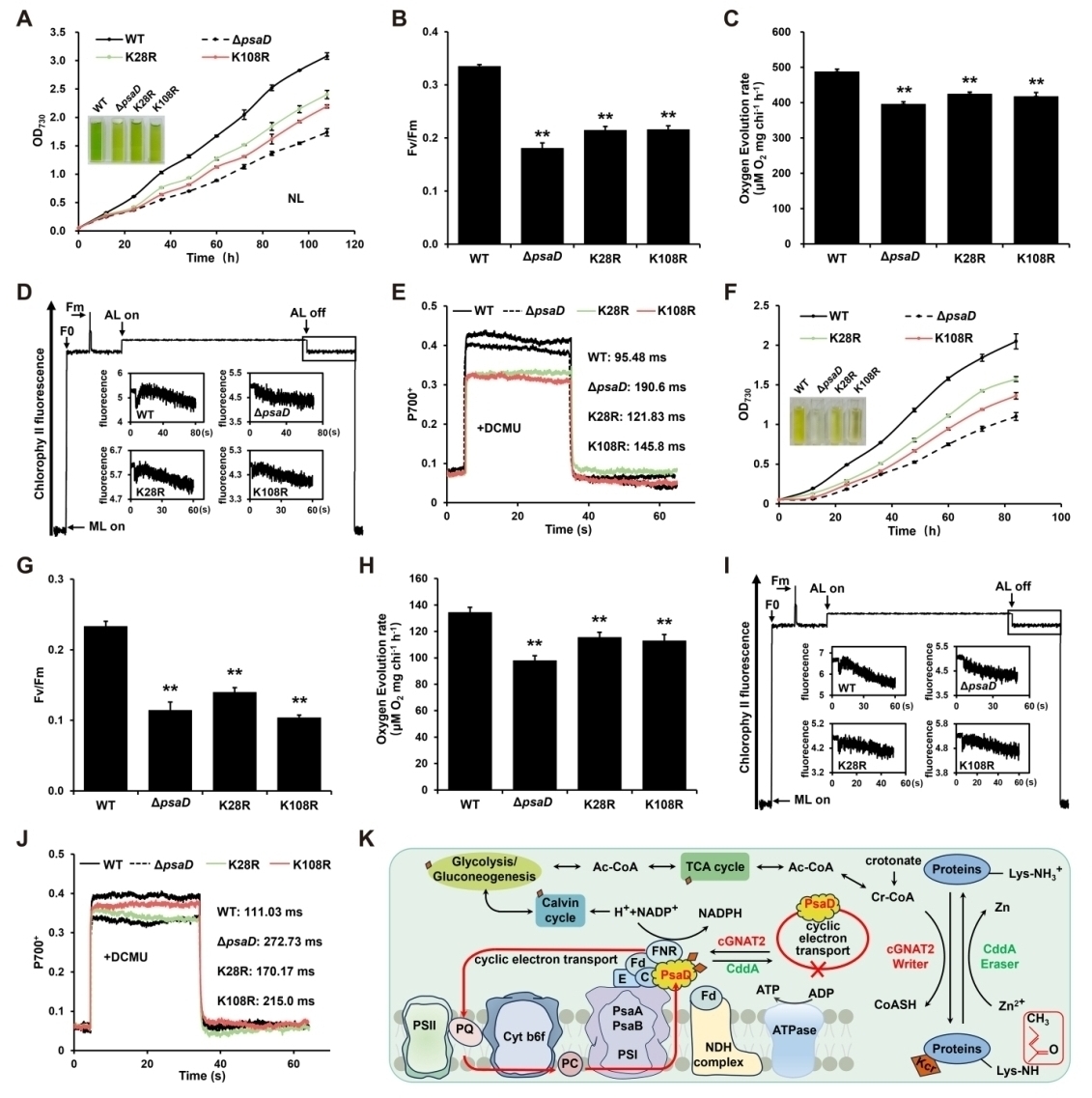
圖5. cGNAT2和CddA在藍細菌中調控生長和光合作用的分子機制模型
該研究成果“The role of CddA and cGNAT2 in crotonylation of proteins in cyanobacteria”在線發表于New Phytologist雜志,水生所博士生林健為該論文的第一作者,葛峰研究員與楊明坤高級實驗師為共同通訊作者,該研究得到自然科學基金和國家重點研發計劃的資助。文章鏈接:https://doi.org/10.1111/nph.70310
